Чтобы внести конкретику, предлагаю рассмотреть свойства бутанола, имеющегося в качестве нежелательной примеси в спирте - сырце.
Бутанол - типичный представитель примесей, составляющих основу "сивухи". Он же - типичный представитель промежуточных примесей.
Имеет температуру кипения 117ОС, и по широко распространенному заблуждению, при ректификации должен попадать в дефлегматор уже после того, как куб покинет весь спирт и вся вода. Но в жизни все не так, как в пособии Прагматехники.
Предлагаю рассмотреть график изменения коэффициента ректификации бутанола в зависимости от концентрации этанола, в котором он содержится в виде примеси.
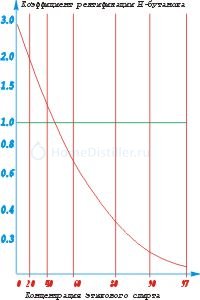 | Позволю себе напомнить что такое коэффициент ректификации и что он означает. Коффициент ректификации численно равен отношению коэффициента испарения примеси к коэффициенту испарения основного вещества. Если коэффициент ректификации (Кр) равен единице, значит содержание примеси в паре будет равно её содержанию в испарявшейся жидкости. Если Кр больше единицы (допустим - 2), значит примесь испаряется вдвое лучше этилового спирта, и её содержание в парах будет вдвое большим, чем в испаряющейся жидкости. Если Кр меньше единицы (например - 0,5), значит примесь испаряется вдвое хуже этилового спирта, и содержание примеся в парах вдаое меньше, чем в жидкости. Мне вроде всё ясно. Надеюсь тому, кто читает, тоже. Прошу обратить особое внимание на то, что температура кипения чистого бутанола (117ОС) не играет абсолютно никакого значения. При кубовой концентрации этилового спирта 20% бутанол испаряется вдвое лучше, чем наш продукт и проявляет свойства головной фракции. |
Rudy, я надеюсь заразить тебя идеей смоделировать потарелочно поведение бутанола. А пока по своему, по-стариковски, на пальцах.
Допустим, мы начинаем ректификацию 40%-ного сырца. Давайте посмотрим по графику как поведет себя бутанол. Куб будет покидать пар, содержание бутанола в котором ненамного выше его содержания в кубе.
На первой же тарелке концентрация этанола составит более 80%. Кр бутанола при такой спиртуозности примерно равен 1/3. Значит с этой тарелки будет испаряться только треть пришедшего туда бутанола. Куда денется остальной? Наверное вернется в куб и снова с паром попадет на первую тарелку.
Давайте покурим - поспим и снова вернемся к нашей колонне. Часть спирта мы уже отобрали, теперь кубовая концентрация этанола стала - скажем - 20%. Теперь бутанол гораздо охотней покидает куб - его испаряемость вдвое больше испаряемости спирта. А что на нашей первой тарелке? 70% этанола, Кр бутанола примерно 1/2. Значит половина этой примеси улетает на вторую тарелку, а оттуда, при спиртуозности 90%, на третью тарелку попадает четверть примеси, и так далее.
Но на 20%-ном содержании спирта в кубе мы не прекращаем ректификацию. Через некоторое время в кубе останется 5% спирта. Кр бутанола достигает уже трёх, и я беру на себя смелость утверждать, что в кубе его больше нет. Слишком хорошо он испаряется по сравнению с этиловым спиртом, а процесс идет уже достаточно долго. Итак, в кубе бутанола уже нет. Так где он? В колонне на тарелках? Может быть. Но я сомневаюсь, что насадочная колонна имеет такую удерживающую способность, что весь бутанол соберется в ней, не проскочив в отбор.
Я предполагаю, что при периодической ректификации проникновение промежуточных фракций в продукт происходит непрерывно в течении всего процесса.
Надо что-то делать. Но что? Пока наиболее эффективное и простое, что приходит в голову - это периодический отбор с нулевым флегмовым числом (в отдельную ёмкость, разумеется). При этом концентрация спирта на тарелках уменьшится и накопившиеся на различных уровнях промежуточные фракции смогут покинуть колонну. После этого нужно дать колонне поработать "на себя" для восстановления рабочего режима и продолжить отбор нормального продукта.
НО...
если бы речь шла только о бутаноле, можно было бы просчитать наиболее эффективный алгоритм такого действия и забыть о бедах. Но этих гадких примесей с коэффициентом ректификации, пересекающим горизонталь "1" достаточно много. Что с ними делать?









