Последние пару недель я много экспериментировал с разными алгоритмами отбора тела. Но, к сожалению, хороший регулятор скорости отбора, поддерживающий температуру датчика в колонне в узком диапазоне (плюс-минус пару квантов DS18B20) и в широком диапазоне спиртуозности в кубе, так пока и не получился. Задача оказалась сложнее, чем представлялась в самом начале. Увы, но на каждый эксперимент уходит день. Само по себе это не страшно - установка работает автоматически, не требует никакого особого внимания и другой работе не мешает. Но если решать эту задачу чисто эмпирически - она может затянуться на многие месяцы. Поэтому я решил отложить ее до лучших времен, пока не будет готова адекватная компьютерная динамическая модель колонны и методика идентификации.
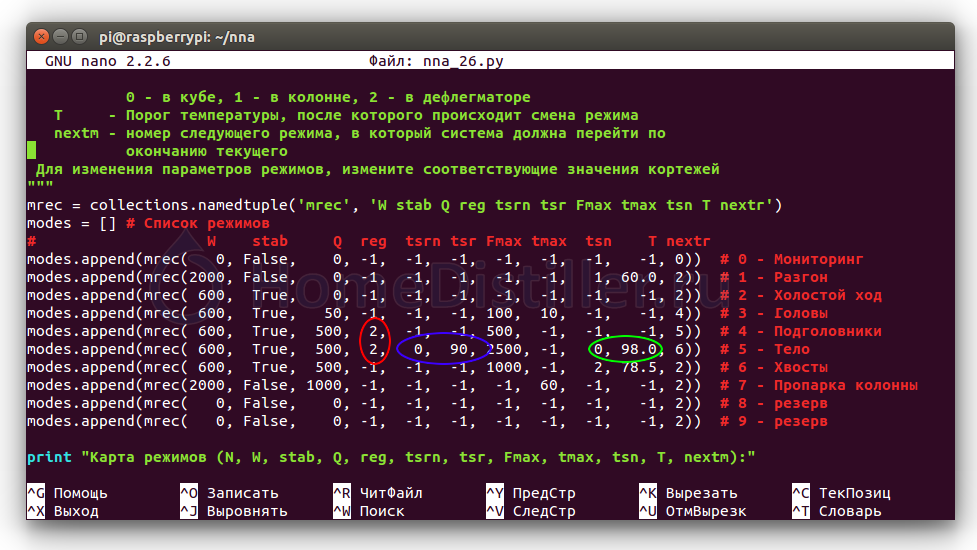
Но, пока суть да дело, хотелось бы чтобы от установки была какая-то реальная польза. В виде готового и хорошего продукта. Т.е. нужны какие-то алгоритмы для практической ректификации. И прямо сейчас. Поэтому я написал и проверил на практике новый скрипт, который реализует два базовых, классических алгоритма ректификации и несколько их комбинаций. Первый базовый алгоритм - это старый-добрый "старт-стоп" и несколько его модификаций. Работа этой группы алгоритмов основана на сравнении температуры, измеренной в определенной точке колонны, с некоторой уставкой. В зависимости от этого сравнения, отбор производится либо с некоторой базовой скоростью, либо полностью прекращается. Работу старт-стопа мы уже рассмотрели здесь достаточно подробно. А следующие два топика будут посвящены другому (тоже довольно популярному) алгоритму, работа которого также основана на измерении температуры, но уже не в колонне или дефлегматоре, а непосредственно в кубе. Сначала немного теории
16.4. Регулирование скорости отбора по температуре в кубе. Теория
Благодаря удачному стечению обстоятельств (точнее - физико-химических свойств этанола, воды и их растворов), поток спирта Qe, поступающего из куба в колонну в виде пара, можно связать очень простым линейным соотношением с разностью температуры кипения чистой воды (100°C) и температуры кипения T раствора спирта в кубе:
Qe = K(P)*(100 - T)*W,
E = Ce*y + Cw*(1-y) - Hсм,
На всякий случай, давайте уточним физический смысл этих вещей. Во-первых, моль - это единица измерения количества вещества. 1 моль = 6.022E+23 молекул вещества (это число еще называют - число Авогадро). Моль - очень удобная единица измерения количества вещества для данной задачи, поскольку он не зависит ни от фазового состояния вещества, ни от химического состава этого вещества. Моль - он и в Африке моль. Это просто количество молекул в штуках :) Ce - энергия, которые нужна для испарения 1 моля спирта (т.е. 6.022E+23 штук молекул спирта) из чистого жидкого спирта. Cw - то же самое, только для чистой воды.
Смысл энтальпии смешения Hсм легко понять, если вспомнить, как сильно нагревается сортировка, когда мы смешиваем спирт с водой. Тепло, которое при этом выделяется - это и есть энергия смешения. А, поскольку сортировку мы обычно делаем при постоянном (атмосферном) давлении, то говорят именно об энтальпии (а не энергии) смешения. Поскольку в паре молекулы разъединены (т.е. больше не взаимодействуют друг с другом), то при испарении раствора мы должны эту энергию как бы "вернуть" системе. Т.е. на испарение раствора спирта в воде нужно затратить энергии больше, чем если бы мы испаряли эквивалентное количества спирта и воды по отдельности. Энтальпия смешения для системы этанол-вода отрицательна, поэтому в формуле выше стоит знак минус.
На рисунке ниже приведена зависимость энтальпии смешения от спиртуозности раствора для атмосферного давления и температуры 25°C. Большое количество эмпирических данных по энтальпиии смешения можно найти в открытом доступе, например, здесь. По части этих данных и был построен график ниже.
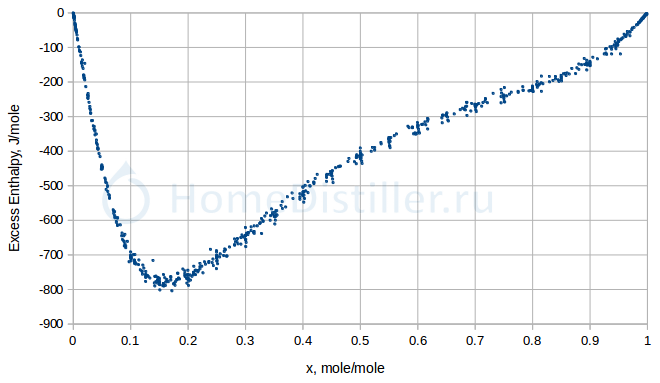
Из рисунка мы видим, что порядок мольной энтальпии смешения - это сотни джоулей на моль (макс. - 800), а порядок мольных теплот испарения (Ce и Cw, приведенные выше) - десятки тысяч джоулей на моль. Т.е. энтальпия смешения вносит лишь небольшой вклад в суммарную энергию, которую необходимо затратить для испарения моля раствора. Hсм << Ce, Cw. Т.е. энергией смешения для нашей задачи мы с чистой совестью можем пренебречь. Далее стОит обратить внимания на второе удачное стечение обстоятельств, заключающееся в том, что мольные теплоты испарения чистого спирта 38560 Дж/моль и чистой воды 40680 Дж/моль очень близки по величине. Т.е. на испарение одной молекулы спирта из чистого спирта требуется примерно столько же энергии, что и для испарения одной молекулы воды из чистой воды. Из этого следует (см. предыдущую формулу), что энергия E, необходимая для образования 1 моля пара практически не будет зависеть от спиртуозности пара y (Ce и Cw близки, значит y почти "сократится"). В результате, мы получим очень простое соотношение для суммарного потока пара Q из куба в колонну в молях за секунду:
Q = (1/C)*W,
Qe = (1/C)*y*W,
В условиях термодинамического равновесия (а наличие локального термодинамического равновесия в нашей системе мы всегда предполагаем) спиртуозность пара однозначно связана со спиртуозностью раствора и, следовательно, с его температурой кипения. Посчитаем и построим график зависимости мольной доли спирта в паре y от разности температуры кипения чистой воды (100) и температуры кипения раствора в кубе. Код на языке Си, при помощи которого можно все это посчитать, я положил в приложение к топику (файл van_Laar_xy.c). График для давления 760 мм.рт.ст. приведен на рисунке ниже.
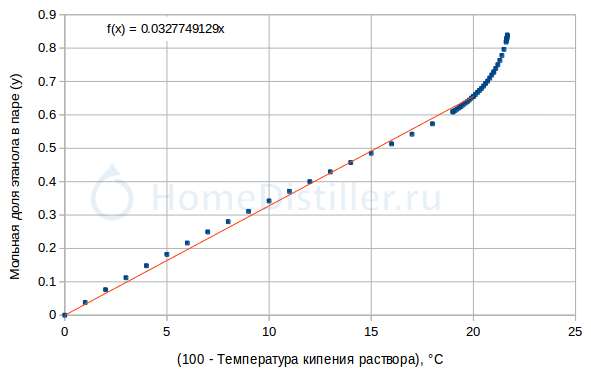
Из графика мы видим, что в диапазоне температуры кипения больше 80°C (т.е. (100-T)<20, что соответствует спиртуозности раствора < 78 об.%, т.е. фактически весь разумный диапазон крепости сырца) кривая хорошо аппроксимируется линейной функцией (красная линия, уравнение регрессии показано слева сверху). Таким образом:
y = 0.0328*(100 - T),
Qe = 0.0328*(1/C)*(100 - T)*W.
Qe = 0.174*(100 - T)*W,
Если теперь мы зададимся конкретным флегмовым числом R, то измерив температуру кипения раствора в кубе и зная мощность нагрева, мы можем сразу же оценить требуемую скорость отбора Qотб, обеспечивающую заданное флегмовое число:
Qотб = 0.174*(100 - T)*W/(R + 1) мл/час.
По сути дела, именно на этой формуле и основан способ регулирования отбора тела по температуре в кубе. Практическую его реализацию мы рассмотрим уже в следующем топике.
Примечание 1. Здесь, на всякий случай уточним. Флегмовое число - это отношение количества флегмы, возвращаемой в колонну из дефлегматора, к количеству флегмы, покидающей колонну в виде конечного продукта. Мы предполагаем, что колонна работает в квазистационарном режиме. Поэтому количество пара, испарившегося из куба и поступившего в колонну в точности равно количеству флегмы, возвращаемой в колонну плюс количество флегмы, отобранной из процесса. Т.е. Qe = Qотб*(R + 1), где R - флегмовое число.
Примечание 2. Этот способ регулирования отбора по температуре куба является довольно приблизительным. Он не содержит обратной связи с какими-нибудь параметрами колонны и/или дефлегматора и не требует их поддержания в относительно узких диапазонах. Поэтому мы здесь не учитываем слабые зависимости температур кипения от давления, которые дают не очень большие поправки и в температуру кипения чистой воды, и в регрессионные коэффициенты.
======================================
Предыдущий топик Вернуться к оглавлению Следующий топик