Инвертирование сахара имеет один недостаток – в процессе вырабатывается канцерогенное вещество фурфурол. И чем дольше идет процесс, тем больше его будет выработано. Поэтому, если принято решение инвертировать сахар, то необходимо найти ту точку, когда инвертирование уже завершается, дабы не вырабатывать вредности больше неизбежного. Исходя из данного материала, которым поделился Daniil [сообщение #13454702] подтверждается вывод, что чем меньше времени инвертируется сахар, тем меньше вредностей. Поэтому поиск оптимального соотношения кислоты, температуры и времени – необходим.
В поисках оптимального соотношения Григорий С поделился ссылкой [сообщение #13455015] на тему, где подробно расписан процесс инвертирования http://www.homebrewer.ru/...ie-saxara.2831/ и размещена интересная номограмма.
Продублирую тут текст работы с номограммой.
Скрытый текст
Инвертирование сахарозы.Источник инвертирования:
- сахароза (тростниковый сахар, свекловичный сахар)
Продукты инвертирования:
- глюкоза
- фруктоза
Что такое инвертирование сахарозы?
Инвертирование столового сахара это реакция гидролиза молекулы сахарозы в кислой среде или в присутствии фермента с общим названием - гидролаза, в результате которой образуется молекула глюкозы и молекула фруктозы.
При этом кислота не расходуется, а выступает только как катализатор.
Это реакция молекулы сахарозы с молекулой воды с увеличением массы конечных продуктов, поэтому из 95 грамм сахарозы получается 100 грамм инвертного сахара.
Также инвертный сахар чуть более сладкий при температуре до 40оС, чем сахароза из-за фруктозы.
Для инвертирования сахарозы, как в домашних условиях, так и на производстве, применяют кислоты.
Можно использовать любую кислоту, если вас интересует этот процесс только с точки зрения химического опыта, но для получения пищевого продукта лучше ограничиться следующим списком кислот:
Молочная кислота
Формула: C3H6O3
Молярная масса: 90,1 г/моль
Плотность: 1,225 г/см³
К1 = 1,38*10−4
Лимонная кислота
Формула: C6H8O7
Молярная масса: 192,1 г/моль
Плотность: 1,66 г/см³
К1 = 7,447*10−4
Ортофосфорная кислота
Формула: H3PO4
Молярная масса: 97,9 г/моль
Плотность: 1,88 г/см³
К1 = 1,1*10−2
Серная кислота
Формула: H2SO4
Молярная масса: 98,1 г/моль
Плотность: 1,84 г/см³
*К1 – константа диссоциации по первой ступени.
Эти кислоты интересны тем, что они нелетучие, первые две пищевые, две последние образуют плохо растворимый осадок при реакции с карбонатом кальция (мелом), который также нетоксичен.
В дальнейшем можно отфильтровать или декантировать сироп от осадка.
Поэтому рекомендуется использовать эти кислоты.
Ряд построен с увеличением эффективности сверху вниз.
Медленнее всего реакция гидролиза будет проходить с молочной кислотой, быстрее всего с серной.
Чем выше температура смеси и ниже показатель pH, тем быстрее протекает реакция гидролиза.
По номограмме можно легко определить количество проинвертировавшей сахарозы.
Для этого надо знать температуру, рН сиропа и продолжительность процесса.
текст
На графике пунктирной линией отображен пример, который показывает 60%-ое разложение сахарозы при +70оС, рН - 2,4, продолжительность процесса 120 минут.
Таким образом нам всего лишь необходимо рассчитать показать pH для того, чтобы определиться, сколько нам потребуется времени для достижения того или иного процента инвертирования сахарозы или исходя из требуемого pH рассчитать количество кислоты.
Определимся с терминами, которые нам потребуются для расчетов.
Молекулярная масса — масса молекулы, выраженная в атомных единицах массы.
Молярная масса — масса вещества в граммах, численно равная молекулярной массе, измеряется в г/моль.
Молярная концентрация — это отношение количества растворенного вещества (в молях) к объему раствора в литрах.
Константа диссоциации (справочная величина) — вид константы равновесия, которая характеризует склонность объекта диссоциировать (разделяться) обратимым образом на частицы
[H+] – концентрация ионов водорода в моль/л.
На примере серной кислоты выясним эти величины.
Формула серной кислоты – H2SO4,
Молекулярная масса – 1*2+32*1+16*4 = 98 (атомные массы берутся из таблицы Д.И. Менделеева)
Молярная масса – 98г/моль
Молярная концентрация – 1 моль/л, это 98 грамм кислоты на литр раствора.
Константа диссоциации равна единице, потому что это сильная кислота.
Как найти концентрацию ионов водорода?
Молекула серной кислоты диссоциирует по формуле:
H2SO4=2H+ + SO4-
Значит из одного моля серной кислоты получается 2 моля ионов водорода.
Получается, что молярная концентрация ионов водорода в два раза больше молярной концентрации серной кислоты.
И если в литре раствора 98 г кислоты, что равно одному молю, то в этом растворе 2 моля ионов водорода. [H+] = 2 моль/л
Водородный показатель pH рассчитывается по формуле: pH= - lg [H+]
получаем, pH= - lg [2] = - 0,3 (ух, очень кислый раствор)
Несмотря на то, что мы привыкли думать о pH в диапазоне от 0 до 14, этот показатель может выходить за эти пределы.
Чтобы понять, сколько молей кислоты надо растворить, зная pH, надо возвести 10 в степень показателя pH с отрицательным знаком.
10 в степени -(-0.3), то есть 10 в степени 0.3 равно 2 моль.
Решим такую задачку:
сколько грамм серной кислоты должно быть в литре раствора, чтобы получить pH=2?
Решение:
1. Находим количество моль ионов водорода
10 в степени -2 равно 0,01 моль
2. Если 1 моль серной кислоты - 98 грамм, то 0,01 это 0,98гр, но так как количество моль ионов
водорода в два раза больше, то кислоты в два раза меньше, то есть 0,49гр.
Получается, чтобы сделать раствор с pH=2, нам нужно взять 0,49 гр. серной кислоты на 1 литр раствора.
-----------------------------------------------------------------------------------------------------------
Для слабых кислот необходимо учитывать константу диссоциации.
Поэтому для них концентрация ионов водорода будет считаться по формуле
[H+] = корню квадратному из произведения Кд на молярную концентрацию.
Решим такую задачу:
Какой величины получится pH если в литре раствора будет 10гр лимонной кислоты?
Решение:
1. Найдем, сколько молей составляют 10 гр. лимонной кислоты.
Молярная масса лимонной кислоты – 194 г/моль, значить 10 гр. это 0,05 моль.
2. Получается что у нас 0,05 молярный раствор.
3. Лимонная кислота диссоциирует по трем ступеням, но нас интересует только первая, так как
вторая и третья значительно меньше и мы ими пренебрежем.
Кд = 7,447⋅10−4 , значит [H+] =√7,447⋅10−4*0,05 = 0,006
4. По формуле рассчета pH= - lg [H+] = 2.2
При растворении 10 грамм лимонной кислоты на литр раствора получаем pH=2.2
--------------------------------------------------------------------------------------------------------------
Зная как найти pH, мы можем воспользоваться номограммой и определить, сколько времени при данном уровне pH для достижения той или иной степени инвертирования сахара.
Применяем знания к процессу инвертирования сахара.
При растворении 2гр лимонной кислоты в литре раствора, получим pH=2,5.
Предположим, что будем нагревать на водяной бане при 95оС чтобы ни в коей мере не получить карамель.
Исходя из номограммы получаем, что при этих условиях необходимо нагревать раствор 55-60 минут.
Также необходимо учитывать, что в случае со слабыми кислотами слишком крепкий раствор сахара будет снижать степень диссоциации кислоты, тем самым изменяя расчетные данные в сторону увеличения показателя pH.
Минирецепты для инвертирования сахара.
С лимонной кислотой:
Сахар – 500 г
Вода – довести объем до 1000 мл
Лимонная кислота – 2 г
Температура – 95оС (водяная баня)
Время нагрева – 60 мин.
С серной кислотой:
Сахар – 500 г
Вода – довести объем до 1000 мл
Серная кислота – 0,15 г
Мел (для гашения кислоты) – 0,2 г
Температура – 95оС (водяная баня)
Время нагрева – 60 мин.
В процессе гашения кислоты образуется – 0,21 г сульфата кальция (гипса)
В дальнейшем можно упарить сироп до нужной вам степени карамелизации или до 70%, не доводя до карамелизации.
Для использования номограммы необходимо в первую очередь определить рН сиропа. Т.к. самая доступная кислота является лимонная, то на ее основе сделал свои расчеты. Если есть желание использовать иные кислоты, то можете сделать свои расчеты по приведенной выше методике.
Для определения рН раствора я использую указанную в методике формулу. Для удобства вставил ее в бражный калькулятор от Abettor, соответствующая тема здесь [Бражный калькулятор] Если используете в работе другие файлы excel то можете использовать готовую формулу и вставить ее в нужное для себя место – «=-LOG(КОРЕНЬ(7,447*СТЕПЕНЬ(10;-4)*((А/(((Б/1,61)+В)/1000))/194)))», где:
А = ячейка с весом лимонной кислоты в гр.
Б = ячейка с весом сахара в гр.
В = ячейка с объемом воды в мл.
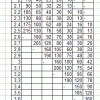
После того как рН раствора определен можно выбрать температуру сиропа. Самое простое – это использовать температуру кипения. Разное количество сахара ведет к разной концентрации сиропа, и температура его кипения будет разная. Табличка прилагается.Об источнике здесь [сообщение #13457429]
Теперь, когда знаем рН сиропа и его температуру кипения, можно использовать номограмму – это сделать просто: выбираете слева температуру, отмечаете точкой, потом отмечаете на соседней шкале точку рН вашего раствора и через эти точки проводите прямую до средней шкалы.
От точки на средней шкале ведете прямую либо через желаемый процент инвертирования, либо через желаемое время инвертирования (шкалы справа от средней).
Таким образом получаете выходные данные по времени и проценту инвертирования.
Например, при соотношении на 1 кг сахара 520мл воды и 0,8 гр лимонной кислоты - рН сиропа будет равен 2,8, а время полного инвертирования составит 42 минуты кипения сиропа (t* кипения 102,5*С для сиропа 55%) и дальнейшее кипение только добавляет вредные вещества.
Проведя некоторое множество вычислений получилась интересная табличка, из которой следует, что достаточным, и значит оптимальным временем для инвертирования, является 15 минут кипения сиропа имеющего рН 2,5. Чтобы получился подобный сироп я использую при инвертировании следующее соотношение (брага 20 л):
1000 мл воды
4300 гр сахара
10 гр. лимонной кислоты. – это не много. т.к. впоследствии сироп будет разбавлен дополнительными 16 л воды (на 20 литров браги) и рН браги станет равен 2,85.
Процесс инвертирования происходит просто: в емкость налить воды, добавить сахар, нагреть. До инвертирования сироп серый, состоит из мелких пузырьков. Как только сироп начинает кипеть, т.е. достигает расчетной температуры - добавляется лимонная кислота. Сразу будет бурная реакция, поэтому надо либо глубокую емкость с высокими бортами (сироп норовит таки убежать), либо пару минут постоянно помешивания до прекращения реакции. Немного принижаем температуру и поддерживаем ее необходимое время. В течение 15-20 минут (при вышеуказанных условиях рН=2,5 t=110*C – расчетное время 13 минут) сироп приобретает соломенный цвет и становится полностью прозрачным. Предлагаемая методика «капля в воду» [сообщение #13454674] подтверждает, что по истечении расчетного времени поведение сиропа в воде перестает изменяться, что также подтверждает окончание инвертирования.
18.04.2019. Обновлен калькулятор









 ) инвертирования составит 42 минуты кипения сиропа" - не понятно...
) инвертирования составит 42 минуты кипения сиропа" - не понятно...

